다국적제약사 아스트라제네카의 코로나19 백신이 국내 보건당국의 시판 전 마지막 품질 검정절차를 통과했다.
식품의약품안전처는 17일 아스트라제네카의 코로나19 백신에 관해 국가출하승인 적합 결정을 내린 것으로 알려졌다.
![아스트라제네카 코로나19 백신, 식약처로부터 국가출하 승인받아]()
백신은 식약처의 품목허가와는 별개로 시판되기 전에 품질을 검증하는 국가출하 승인절차를 거쳐야 한다.
아스트라제네카의 코로나19 백신은 10일 식약처로부터 임상3상 시험결과를 제출하는 조건으로 품목허가를 받은 뒤 국가출하 승인절차를 밟아왔다.
식약처는 품목허가를 신청한 화이자의 코로나19 백신에 관해서는 3월 첫째 주 이후에 품목허가 여부를 결정한다는 계획을 세웠다.
화이자 백신의 품목허가 심사를 위해 2월 넷째 주 이후 전문가 자문회의를 진행하기로 했다. [비즈니스포트스 최영찬 기자]
식품의약품안전처는 17일 아스트라제네카의 코로나19 백신에 관해 국가출하승인 적합 결정을 내린 것으로 알려졌다.
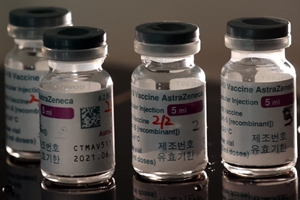
▲ 다국적 제약사 아스트라제네카의 코로나19 백신 사진. <연합뉴스>
백신은 식약처의 품목허가와는 별개로 시판되기 전에 품질을 검증하는 국가출하 승인절차를 거쳐야 한다.
아스트라제네카의 코로나19 백신은 10일 식약처로부터 임상3상 시험결과를 제출하는 조건으로 품목허가를 받은 뒤 국가출하 승인절차를 밟아왔다.
식약처는 품목허가를 신청한 화이자의 코로나19 백신에 관해서는 3월 첫째 주 이후에 품목허가 여부를 결정한다는 계획을 세웠다.
화이자 백신의 품목허가 심사를 위해 2월 넷째 주 이후 전문가 자문회의를 진행하기로 했다. [비즈니스포트스 최영찬 기자]




![[여론조사꽃] 이재명 지지율 73.6%로 2.9%p 내려, 민주당 55.9% vs 국힘 24.5%](https://businesspost.co.kr/news/photo/202605/20260511111534_53025.jpg)






