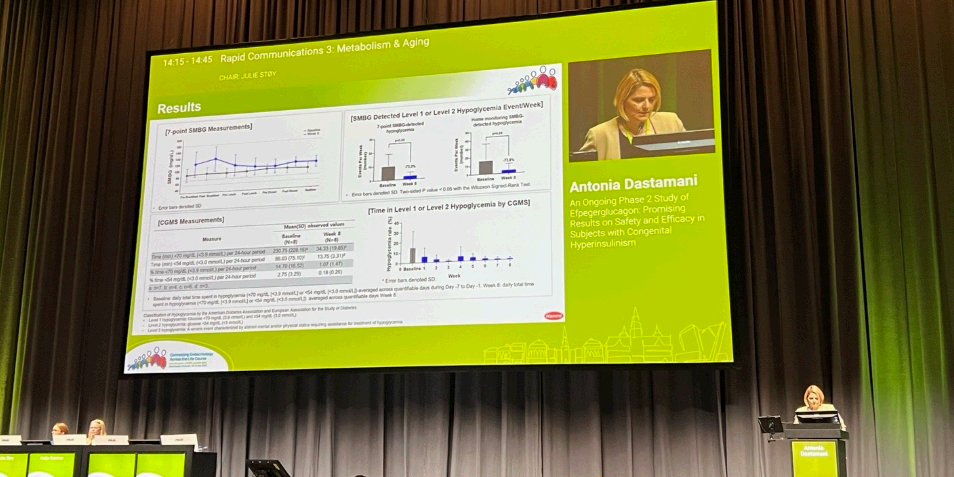
▲ 안토니아 다스타마니 박사가 11일(현지시각) 덴마크 코펜하겐에서 열린 유럽소아내분비학회(ESPE) 및 유럽내분비학회(ESE) 공동 학술대회에서 에페거글루카곤에 대한 임상2상 중간 분석 결과를 발표하고 있다. <한미약품>
한미약품은 10일부터 13일까지 덴마크 코펜하겐에서 열린 유럽소아내분비학회(ESPE) 및 유럽내분비학회(ESE) 공동 학술대회에 참가해 에페거글루카곤의 임상2상 중간 분석 결과를 구두 및 포스터 발표를 통해 공개했다고 26일 밝혔다.
선천성 고인슐린증은 인슐린이 과도하게 분비돼 저혈당증을 유발하는 희귀질환이다. 2만5천 명~5만 명당 1명 꼴로 발병하며 해마다 미국과 유럽에서는 약 300명의 신규 환자들이 진단되고 있다.
현재까지 승인된 치료제(1건)가 있긴 하지만 치료 반응이 특정 유전자형에 한정되고 부작용(다모증, 체액 저류, 심부전 등)이 많아, 환자들은 허가 이외의 의약품을 사용하거나 부작용을 감수하고 췌장을 절제하는 수술에 의존하고 있다고 한미약품은 설명했다.
한미약품은 선천성 고인슐린증 치료제 ‘에페거글루카곤’을 세계 최초 주 1회 투여 제형으로 개발하고 있다. 현재 5개 나라에서 글로벌2상이 진행되고 있으며, 국내에서는 최진호 서울아산병원 소아청소년과 교수가 임상 연구자로 참여하고 있다.
한미약품에 따르면 에페거글루카곤은 안전성과 내약성이 우수하며 활력 징후와 신체 검사, 안전성 실험실 검사, 심전도에서 특이사항이 발견되지 않았다. 또한 치료를 중단해야 하는 부작용이나 특별히 우려할 부작용은 보고되지 않았다.
전체 투여 기간 동안 주당 저혈당(혈당 70㎎/dL 미만) 및 심각한 저혈당(혈당 54㎎/dL 미만) 발생 횟수와 시간이 유의미하게 감소했으며 특히 8주 후에는 70㎎/dL 미만의 저혈당이 72.3%, 54㎎/dL 미만의 심각한 저혈당은 87.5% 감소하는 효과를 보였다. 약물의 8주 차 평균 반감기는 89시간으로 나타나 주 1회 투약 간격을 뒷받침하는 결과가 확인됐다.
한미약품의 임상 연구를 진행하는 영국 그레이트 오몬드 스트리트 병원의 연구자인 안토니아 다스타마니 박사는 “에페거글루카곤은 주 1회 투여만으로도 저혈당 발생 위험을 크게 감소시키는 유망한 신약”이라며 “환자들에게 새로운 치료 대안이 되길 고대한다”고 말했다. 김민정 기자




![[여론조사꽃] 이재명 지지율 73.6%로 2.9%p 내려, 민주당 55.9% vs 국힘 24.5%](https://businesspost.co.kr/news/photo/202605/20260511111534_53025.jpg)






